KALKULATOR OKSIDACIJSKIH BROJEVA
Kako bi izračunali oksidacijske brojeve elemenata u kemijskom spoju unesite njegovu formulu u polje za unos i kliknite 'Izračunaj' (na primjer: Ca2+, HF2^-, Fe4[Fe(CN)6]3, NH4NO3, so42-, ch3cooh, cuso4*5h2o).
| Element: | Cu | S | O | * | H | O |
| Oksidacijski broj: | +2 | +6 | -2 | +1 | -2 |
Stupanj oksidacije je naboj koji bi ostao na promatranom atomu ako bi zajednički elektronski parovi pripali elektronegativnijem atomu. Oksidacijski broj je sinonim za stupanj oksidacije. Određivanje oksidacijskih brojeva iz Lewisovih struktura (slika 1a) mnogo je jednostavnije nego određivanje iz molekularne formule (slika 1b). Oksidacijski broj svakog atoma izračuna se tako da se od broja valentnih elektrona oduzme zbroj slobodnih elektronskih parova i elektrona dobivenih privlačenjem zajedničkih elektronskih parova. Elektroni u vezama između atoma istog elementa (homonuklearne veze) dijele se jednako na oba atoma.
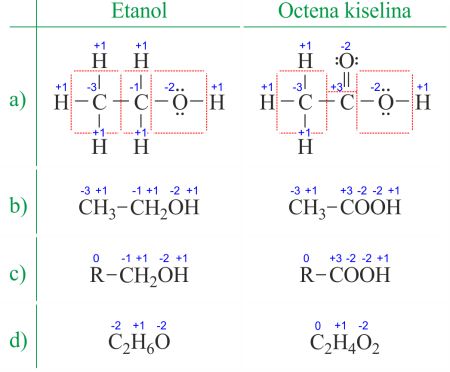
Kad se radi s organskim spojevima i formulama s više istovrsnih atoma lakše je raditi s molekularnim formula i prosječnim oksidacijskim brojevima (slika 1d). Organski spojevi mogu se pisati i na način da se sve što se ne mijenja do prve C-C veze zamijeni kraticom R (slika 1c). Za razliku od radikala u organskoj kemiji, R ne može biti vodik. Kako su između dva atoma ugljika elektroni jednako podijeljeni R skupina ne mijenja oksidacijski broj ugljikovog atoma na koji je vezana. Primjer upotrebe možete pronaći na stranici Dijeljenje redoks reakcije u dvije parcijalne reakcije.
Pravila za određivanje oksidacijskih brojeva
- Oksidacijski broj atoma svih elemenata u elementarnom stanju je nula (0).
- Stupanj oksidacije monoatomnog iona jednak je naboju tog iona.
- Fluor, kao najelektronegativniji element, u svim spojevima uvijek ima stupanj oksidacije -1.
- Alkalijski metali u svim spojevima imaju stupanj oksidacije +1.
- Zemnoalkalijski metali u svim spojevima imaju stupanj oksidacije +2.
- Oksidacijski broj kisika u većini spojeva je -2, osim u peroksidima (H2O2) gdje je oksidacijski broj kisika -1 i u spojevima s fluorom (OF2) gdje je +2.
- Oksidacijski broj vodika u spojevima je +1 osim u hidridima metala (NaH, MgH2), gdje je oksidacijski broj vodika -1.
- Suma stupnjeva oksidacije atoma svih elemenata koji izgrađuju neutralnu molekulu mora biti jednaka nuli.
- Suma svih oksidacijskih brojeva elemenata u kompleksnim ionima ili radikalima mora biti jednaka naboju iona ili radikala.
Određivanje oksidacijskih brojeva u organskim spojevima
- U organskim spojevima oksidacijski broj ugljika se određuje tako da se ugljiku za svaku vezu sa elektropozitivnijim atomom (H, Na, Ca, B) pridoda -1 a za svaku vezu sa elektronegativnijim atomom (O, Cl, N, P) pridoda +1. Na primjer:
- propen: CH3-CH=CH2
- laurinska kiselina: CH3(CH2)10COOH
- di-terc-butil peroksid: (CH3)3COOC(CH3)3
- diizopropil eter: (CH3)2CH-O-CH(CH3)2
- dibenzil sulfid: (C6H5CH2)2S
- cistein: HO2CCH(NH2)CH2SH
Citiranje ove stranice:
Generalić, Eni. "Kalkulator oksidacijskih brojeva." EniG. Periodni sustav elemenata. KTF-Split, 13 Feb. 2025. Web. 2 Apr. 2025. <https://www.periodni.com/hr/kalkulator_oksidacijskih_brojeva.php>.
Članci i tablice
- Periodni sustav
- Home
- Kratki oblik tablice periodnog sustava
- Dugi oblik tablice periodnog sustava
- Povijest periodnog sustava kemijskih elemenata
- Printabilni periodni sustav
- Elektronske konfiguracije elemenata
- Abecedni popis kemijskih elemenata
- Imenovanje elemenata s atomskim brojem većim od 100
- ASCII Periodni sustav
- Online kalkulatori
- Znanstveno računalo (kalkulator) za kemičare
- Kalkulator plinskih zakona
- Kalkulator molarne mase
- Pretvaranje kutova
- Pretvaranje rimskih brojeva u arapske
- Pretvaranje brojevnih sustava
- Priprema otopina
- Označavanje kemijskih posuda
- Kalkulator oksidacijskih brojeva
- ARS metoda
- Metoda promjene oksidacijskih brojeva
- Ion-elektron metoda
- Gaussova metoda eliminacije
- Igra memorije
- Pronađi parove
- Članci i tablice
- Kemija
- Lista kratica i akronima
- Kristalni sustavi i Bravaisove rešetke
- GHS - Piktogrami opasnosti
- NFPA 704 dijamant opasnosti
- Temeljne fizikalne konstante
- Konstante produkta topljivosti
- SI - Međunarodni sustav mjernih jedinica
- Sastav smjesa i otopina
- Stehiometrijski račun
- Klorinitet i slanost mora
- Elementi rijetkih zemalja (REE)
- Izjednačavanje kemijskih jednadžbi
- Teorija valentne veze
- Ekologija
- Web dizajn
- Kemijski rječnik
- Kemija
- Download
- ≡ Meni
