Mn
Manganum
MANGANESO
ELEMENTOS DE TRANSICIÓN: GRUPO DEL MANGANESO
| Número atómico: | 25 |
| Grupo: | 7 |
| Periodo: | 4 |
| Configuración electrónica: | [Ar] 3d5 4s2 |
| Estados de oxidación: | +2 +3 +4 +7 |
| Electronegatividad: | 1.55 |
| Radio atómico / pm: | 136.7 |
| Masa atómica relativa: | 54.938 044(3) |
El manganeso fue descubierto en 1774 por Scheele en el mineral pirolusita, variedad natural de dióxido de manganeso, llamada 'magnesia negra', de donde proviene su denominación. Es un metal duro de color blanco de plata. Muy difundido en la naturaleza, forma concentraciones de pirolusita negra en los sedimentos marinos. Se emplea en la metalurgia para mejorar la calidad del acero, en la industria de colorantes y en otras muchas industrias químicas.
| Densidad / g dm-3: | 7440 | (alfa, 293 K) |
| 6430 | (m.p.) | |
| Volumen molar / cm3mol-1: | 7.38 | (alfa, 293 K) |
| 8.54 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 144 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 7.82 |
| Punto de fusión / °C: | 1246 |
| Punto de ebullición / °C: | 2061 |
| Calor de fusión / kJ mol-1: | 14.4 |
| Calor de vaporización / kJ mol-1: | 220.5 |
| Calor de atomización / kJ mol-1: | 279.37 |
| Primera energía de ionización / kJ mol-1: | 717.28 |
| Segunda energía de ionización / kJ mol-1: | 1509.04 |
| Tercera energía de ionización / kJ mol-1: | 3248.49 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 1400 |
| en los océanos / ppm: | 0.002 |
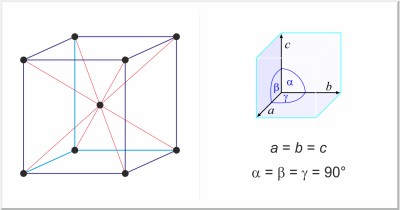
| Estructura cristalina: | cúbica centrada en el cuerpo |
| Dimensiones de la celda unidad / pm: | a=891.39 |
| Grupo espacial: | I43m |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 55Mn | 54.938050(1) | 100 |
| Semirreacción | Eo / V | |
|---|---|---|
| MnIV + e- → MnIII | +1.65 | (14 mol dm-3 H2SO4) |
| MnIII + e- → MnII | +1.59 | (14 mol dm-3 H2SO4) |
| Mn3+ + e- → Mn2+ | +1.51 | (7.5 mol dm-3 H2SO4) |
| Mn2+ + 2e- → Mn(s) | - 1.180 | |
| MnO4- + e- → MnO42- | +0.564 | |
| MnO4- + 2H2O + 3e- → MnO2(s) + 4OH- | +0.588 | |
| MnO4- + 4H+ + 3e- → MnO2(s) (alfa) + 2H2O | +1.695 | |
| MnO4- + 4H+ + 3e- → MnO2(s) (beta) + 2H2O | +1.679 | |
| MnO4- + 8H+ + 4e- → Mn3+ + 4H2O | +1.506 | |
| MnO4- + 8H+ + 5e- → Mn2+ + 4H2O | +1.51 | |
| MnO42- + 4H+ + 2e- → MnO2(s) + 2H2O | +2.257 | |
| MnO42- + 5H+ + 2e- → HMnO2- + 2H2O | +1.234 | |
| MnO42- + 2H2O + 2e- → MnO2(s) + 4OH- | +0.51 | (18 °C) |
| MnO2(s) + 4H+ + e- → Mn3+ + 2H2O | +0.948 | |
| MnO2(s) (alfa) + 4H+ + 2e- → Mn2+ + 2H2O | +1.23 | |
| MnO2(s) (beta) + 4H+ + 2e- → Mn2+ + 2H2O | +1.22 | |
| MnO2(s) (gamma) + 4H+ + 2e- → Mn2+ + 2H2O | +0.21 | |
| Mn(OH)3(s) + e- → Mn(OH)2(s) + 2OH- | +0.1 | |
| Mn(CN)63- + e- → Mn(CN)64- | - 0.244 | |
| Mn(OH)2(s) + 2e- → Mn(s) + 2OH- | - 1.55 | |
| HMnO2- + 3H+ + 2e- → Mn(s) + 2H2O | - 0.163 |
Citación de esta página:
Generalic, Eni. "Manganeso." EniG. Tabla periódica de los elementos. KTF-Split, 13 Feb. 2025. Web. 13 Apr. 2025. <https://www.periodni.com/es/mn.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
Copyright © 1998-2025 by Eni Generalic. Todos los derechos reservados. | Bibliografía | Disclaimer
