CALCIUM
MÉTAL ALCALINO-TERREUX
| Nombre atomique: | 20 |
| Groupe: | 2 |
| Période: | 4 |
| Configuration électronique: | [Ar] 4s2 |
| Nombre d'oxydation: | +2 |
| Électronégativité: | 1 |
| Rayon atomique / pm: | 197.4 |
| Masse atomique relatives: | 40.078(4) |
Le calcium a été découvert par Sir Humphry Davy (GB) en 1808. Étymologie du nom: vient du latin calx signifiant chaux. Le calcium est un métal gris-blanc, assez dur. Les surfaces au contact de l'air se recouvrent d'une couche d'oxyde et de nitrure. Dans la nature il n'existe que sous forme de composés. Le calcium est obtenu à partir de minerais: craie, pierre à chaux, marbre. Le métal pur est obtenu en faisant réagir de la chaux (CaCO3) avec de l'aluminium à chaud et sous faible pression. Le calcium est utilisé par plusieurs formes de vie pour fabriquer des coquilles, des arêtes ou des os. Pratiquement on ne se sert pas du métal pur. Deux de ses composés, la chaux (CaO) et le plâtre (CaSO4) sont employés par un grand nombre d'industries.
| Densité / g dm-3: | 1550 | (293 K) |
| 1365 | (m.p.) | |
| Volume molaire / cm3mol-1: | 25.86 | (293 K) |
| 29.36 | (m.p.) | |
| Résistivité électrique / µΩcm: | 3.91 | (20 °C) |
| Conductibilité thermique / W m-1K-1: | 190 |
| Point de fusion / °C: | 842 |
| Point d'ébullition / °C: | 1484 |
| Enthalpie de fusion / kJ mol-1: | 9.33 |
| Enthalpie d'évaporation / kJ mol-1: | 150.6 |
| Chaleur d'atomisation / kJ mol-1: | 177.74 |
| Energie de première ionisation / kJ mol-1: | 589.83 |
| Energie de deuxième ionisation / kJ mol-1: | 1145.46 |
| Energie de troisième ionisation / kJ mol-1: | 4912.40 |
| dans l'atmosphère / ppm: | - |
| dans la croute terrestre / ppm: | 52900 |
| dans les océans / ppm: | 400 |
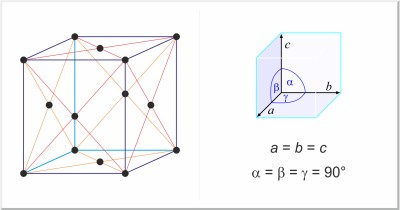
| Structure cristalline: | cubique à faces centrées |
| Dimension de la cellule unitaire / pm: | a=558.84 |
| Groupe d'espace: | Fm3m |
| Isotope | Masse atomique relatives | Pourcentage massique (%) |
|---|---|---|
| 40Ca | 39.9625911(3) | 96.941(18) |
| 42Ca | 41.9586183(4) | 0.647(9) |
| 43Ca | 42.9587668(5) | 0.135(6) |
| 44Ca | 43.9554811(9) | 2.086(12) |
| 46Ca | 45.953693(3) | 0.004(3) |
| 48Ca | 47.952534(4) | 0.187(4) |
| Demi-réaction | Eo / V | |
|---|---|---|
| Ca2+ + 2e- → Ca(s) | - 2.866 | |
| CaO + 2H+ + 2e- → Ca(s) + H2O | - 1.90 | |
| Ca(OH)2(s) + 2e- → Ca(s) + 2OH- | - 3.03 |
| 19 Potassium | ← | 20 Calcium | → | 21 Scandium |
Citation de cette page:
Generalic, Eni. "Calcium." EniG. Tableau périodique des éléments. KTF-Split, 13 Feb. 2025. Web. 31 Mar. 2025. <https://www.periodni.com/fr/ca.html>.
Tableaux et articles
- Tableau périodique
- Home
- Forme courte du tableau périodique
- Forme longue du tableau périodique
- History of the Periodic table of elements
- Impression du tableau périodique
- Configuration électronique des éléments
- Liste alphabétique des éléments chimiques
- Naming of elements of atomic numbers greater than 100
- ASCII Tableau périodique
- Calculatrices online
- Calculatrice scientifique pour chimiste
- Calculatrice lois de gaz
- Calculateur de masse molaire
- Convertir angle
- Convertisseur chiffres romains
- Convertisseur systèmes numériques
- Préparation des solutions
- Étiquetage des conteneurs chimiques
- Calculateur de nombres d'oxydation
- ARS methode
- Méthode du changement des nombres d'oxydation
- Méthode ions-électrons
- Méthode d'élimination de Gauss
- Jeu de mémoire
- Trouvez les paires
- Tableaux et articles
- Chimie
- Liste des abréviations et acronymes
- Systèmes cristallins et réseaux de Bravais
- SGH - Pictogrammes de danger
- NFPA 704 feu diamant
- Constantes physiques fondamentales
- Constantes du produit de solubilité
- SI - Système international d'unités
- Composition des melanges et des solutions
- Calcul stœchiométrique
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Écologie
- Web design
- Dictionnaire de chimie (anglais-croate)
- Chimie
- Télécharger
- ≡ Menu
