IRIDIJ
PRIJELAZNI ELEMENT: SKUPINA KOBALTA
| Atomski broj: | 77 |
| Skupina: | 9 |
| Perioda: | 6 |
| Elektronska konfiguracija: | [Xe] 4f14 5d7 6s2 |
| Oksidacijski broj: | +3 +4 |
| Elektronegativnost: | 2.2 |
| Atomski radijus / pm: | 135.7 |
| Relativna atomska masa: | 192.217(3) |
Iridij je 1803. godine otkrio Smithson Tennant (GB). Ime je dobio po latinskoj riječi iris što znači duga jer su mu spojevi jako obojeni. To je sjajni, vrlo tvrdi, srebrni metal. Zajedno s osmijem i platinom čini skupinu teških platinskih metala. Ni jedna vodena otopina ga ne napada. Razara ga tek rastaljena lužina. Na zraku se nezaštićen može zagrijati do 2300°C. Zbog njegove otpornosti na koroziju, od njegove legure je izrađen prametar (90% Pt i 10% Ir). U prirodi se pojavljuje obično kao pratitelj bakarnih i nikalnih ruda, ili kao osmiridij (prirodna legura osmija i iridija) koja sadrži rutenij. Upotrebljava se za legiranje platine i paladija (povećava im tvrdoću). Cijena spužvastog iridija čistoće 99.95% iznosi 829.60 € za 10 g.
| Gustoća / g dm-3: | 22420 | (290 K) |
| 20000 | (t.t.) | |
| Molarni volumen / cm3mol-1: | 8.57 | (290 K) |
| 8.74 | (t.t.) | |
| Električna otpornost / µΩcm: | 5.3 | (20 °C) |
| Toplinska vodljivost / W m-1K-1: | 147 |
| Temperatura taljenja / °C: | 2446 |
| Temperatura vrenja / °C: | 4428 |
| Toplina taljenja / kJ mol-1: | 26.4 |
| Toplina isparavanja / kJ mol-1: | 612.1 |
| Toplina atomiziranja / kJ mol-1: | 664.34 |
| Prva energija ionizacije / kJ mol-1: | 865.19 |
| Druga energija ionizacije / kJ mol-1: | - |
| Treća energija ionizacije / kJ mol-1: | - |
| u atmosferi / ppm: | - |
| u Zemljinoj kori / ppm: | 0.0001 |
| u oceanima / ppm: | - |
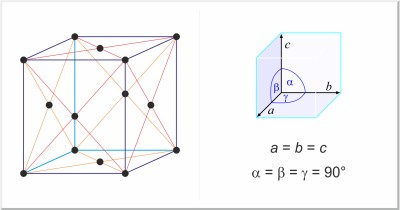
| Kristalna struktura: | plošno centrirana kubična |
| Dimenzije jedinične ćelije / pm: | a=383.92 |
| Prostorna grupa: | Fm3m |
| Izotop | Relativna atomska masa | Maseni udio (%) |
|---|---|---|
| 191Ir | 190.960591(3) | 37.3(5) |
| 193Ir | 192.962924(3) | 62.7(5) |
| Uravnotežena polureakcija | Eo / V | |
|---|---|---|
| Ir3+ + 3e- → Ir(s) | +1.15 | |
| IrCl62- + e- → IrCl63- | +1.026 | |
| IrCl62- + 4e- → Ir(s) + 6Cl- | +0.835 | |
| IrCl63- + 3e- → Ir(s) + 6Cl- | +0.77 | |
| IrO2(s) + 4H+ + 4e- → Ir(s) + H2O | +0.93 | |
| IrO2(s) + 2H2O + 4e- → Ir(s) + 4OH- | +0.1 | |
| Ir2O3 + 3H2O + 6e- → 2Ir(s) + 6OH- | +0.1 |
| 76 Osmij | ← | 77 Iridij | → | 78 Platina |
Citiranje ove stranice:
Generalić, Eni. "Iridij." EniG. Periodni sustav elemenata. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/hr/ir.html>.
Članci i tablice
- Periodni sustav
- Home
- Kratki oblik tablice periodnog sustava
- Dugi oblik tablice periodnog sustava
- Povijest periodnog sustava kemijskih elemenata
- Printabilni periodni sustav
- Elektronske konfiguracije elemenata
- Abecedni popis kemijskih elemenata
- Imenovanje elemenata s atomskim brojem većim od 100
- ASCII Periodni sustav
- Online kalkulatori
- Znanstveno računalo (kalkulator) za kemičare
- Kalkulator plinskih zakona
- Kalkulator molarne mase
- Pretvaranje kutova
- Pretvaranje rimskih brojeva u arapske
- Pretvaranje brojevnih sustava
- Priprema otopina
- Označavanje kemijskih posuda
- Kalkulator oksidacijskih brojeva
- ARS metoda
- Metoda promjene oksidacijskih brojeva
- Ion-elektron metoda
- Gaussova metoda eliminacije
- Igra memorije
- Pronađi parove
- Članci i tablice
- Kemija
- Lista kratica i akronima
- Kristalni sustavi i Bravaisove rešetke
- GHS - Piktogrami opasnosti
- NFPA 704 dijamant opasnosti
- Temeljne fizikalne konstante
- Konstante produkta topljivosti
- SI - Međunarodni sustav mjernih jedinica
- Sastav smjesa i otopina
- Stehiometrijski račun
- Klorinitet i slanost mora
- Elementi rijetkih zemalja (REE)
- Izjednačavanje kemijskih jednadžbi
- Teorija valentne veze
- Ekologija
- Web dizajn
- Kemijski rječnik
- Kemija
- Download
- ≡ Meni
