VANADIUM
UEBERGANGSELEMENTE: VANADIUMGRUPPE
| Ordnungszahl: | 23 |
| Elementgruppen: | 5 |
| Perioden: | 4 |
| Elektronenkonfiguration: | [Ar] 3d3 4s2 |
| Oxidationszustände: | +2 +3 +4 +5 |
| Elekronegativität: | 1.63 |
| Atomradius / pm: | 131.1 |
| Relative atommasse: | 50.9415(1) |
Endeckung:1801 Andres Manuel del Rio (MX)
Das Element Vanadium wurde nach dem Freya (Vanadis), der nordischen Göttin der Schönheit; nach dem farbenprächtigen Aussehen mancher Vanadiumverbindungen. Vanadium ist ein stahlgraues Metall von großer Härte, widerstandsfähig gegenüber starken Säuren und wässrigen Alkalilaugen. Ein bei Mineraliensammlern bekanntes Vanadiumerz ist der Vanadinit. Durch das Rösten oder das Auslaugen von Vanadiumerzen oder vanadiumhaltiger Schlacken erhält man Vanadium(V)-oxid. Vanadium ist ein wichtiges Legierungsmetall in Baustählen und Werkzeugstählen.
| Dichte / g dm-3: | 6110 | (292 K) |
| 5550 | (m.p.) | |
| Atomvolumen / cm3mol-1: | 8.34 | (292 K) |
| 9.18 | (m.p.) | |
| Elektrische widerstandskraft / µΩcm: | 19.68 | (20 °C) |
| Wärmeleitfähigkeit / W m-1K-1: | 30.7 |
| Schmelzpunkt / °C: | 1910 |
| Siedepunkt / °C: | 3407 |
| Bildungsenergie / kJ mol-1: | 17.6 |
| Verdampfungsenergie / kJ mol-1: | 459.7 |
| Zerstäubungsenergie / kJ mol-1: | 510.95 |
| Erste ionisierungenergie / kJ mol-1: | 650.92 |
| Zweite ionisierungenergie / kJ mol-1: | 1414.49 |
| Dritte ionisierungenergie / kJ mol-1: | 2828.10 |
| in der Atmosphäre / ppm: | - |
| in der Erdkruste / ppm: | 230 |
| in den Ozeanen / ppm: | 0.002 |
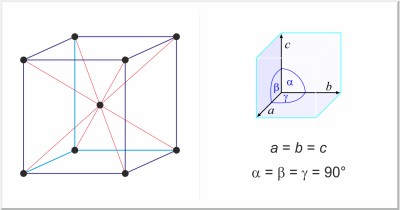
| Kristallstruktur: | kubisch-raumzentriert |
| Gitterparameter der Elementarzelle / pm: | a=302.40 |
| Raumgruppe: | Im3m |
| Isotopen | Relative atommasse | Massenanteil (%) |
|---|---|---|
| 50V | 49.947163(1) | 0.250(2) |
| 51V | 50.943964(1) | 99.750(2) |
| Ausgeglichene halbreaktion | Eo / V | |
|---|---|---|
| V3+ + e- → V2+ | - 0.256 | |
| V3+ + e- → V2+ | - 0.21 | (1 mol dm-3 HClO4) |
| V2+ + 2e- → V(s) | - 1.18 | |
| 2VO43- + 10H+ + 4e- → V2O3 + 5H2O | +1.238 | |
| VO43- + 6H+ + 2e- → VO+ + 3H2O | +1.256 | |
| VO2+ + 2H+ + e- → VO2+ + H2O | +1.00 | |
| V2O5 + 6H+ + 2e- → 2VO2+ + 3H2O | +0.998 | |
| V2O4 + 4H+ + 2e- → 2VO+ + 2H2O | +0.246 | |
| VO2+ + 2H+ + e- → V3+ + H2O | +0.359 | |
| VO2+ + H+ + e- → VOH2+ | +0.164 | |
| VO2+ + e- → VO+ | - 0.044 | |
| V2O3 + 6H+ + 2e- → 2V2+ + 3H2O | +0.161 | |
| VO+ + 2H+ + e- → V2+ + H2O | +0.126 | |
| VOH2+ + H+ + e- → V2+ + H2O | - 0.082 | |
| V(OH)4+ + 2H+ + e- → VO2+ + 3H2O | +1.00 | |
| V(OH)4+ + 2H+ + e- → VO2+ + 3H2O | +1.02 | (1 mol dm-3 HCl) |
| V(OH)4+ + 2H+ + e- → VO2+ + 3H2O | +1.02 | (1 mol dm-3 HClO4) |
Zitieren dieser Seite:
Generalic, Eni. "Vanadium." EniG. Periodensystem der Elemente. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/de/v.html>.
Tabellen und Artikel
- Periodensystem
- Online-Taschenrechner
- Wissenschaftlicher Rechner für Chemiker
- Gasgesetzen Rechner
- Molmassenrechner
- Winkelkonverter
- Römische Zahlen umwandeln
- Numerische Systeme konvertieren
- Herstellung von Lösungen
- Kennzeichnung von Chemikalienbehältern
- Oxidationszahlen Rechner
- ARS methode
- Oxidationszahlmethode
- Ionen-Elektronen-Methode
- Eliminationsmethode von Gauss
- Memory-Spiel
- Paare finden
- Tabellen und Artikel
- Chemie
- Liste mit Akronyme und Abkürzungen
- Kristallsysteme und Bravais-Gitter
- GHS - Gefahrenpiktogramme
- NFPA 704 Gefahrendiamant
- Fundamentale Physikalische Konstanten
- Löslichkeitsprodukt-Konstante
- SI - Internationale Einheitensystem
- Zusammensetzung von Mischungen und Lösungen
- Stöchiometrische Rechnung
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ökologie
- Webdesign
- Chemiewörterbuch (Englisch-Kroatisch)
- Chemie
- Downloads
- ≡ Menü
