Zn
Zincum
ZINK
UEBERGANGSELEMENTE: ZINKGRUPPE
| Ordnungszahl: | 30 |
| Elementgruppen: | 12 |
| Perioden: | 4 |
| Elektronenkonfiguration: | [Ar] 3d10 4s2 |
| Oxidationszustände: | +2 |
| Elekronegativität: | 1.65 |
| Atomradius / pm: | 133.5 |
| Relative atommasse: | 65.38(2) |
Endeckung:- -
Der Name Zink kommt vom von deutsche 'Zinken' (da Zink zackenförmig erstarrt). Es ist ein bläulich glänzendes, bei Raumtemperatur relativ sprödes Schwermetall. In der Natur findet sich kein elementares Zink. Die beiden wichtigsten Zinkerze sind Zinkblende und Zinkspat. Aufbereitung des Kupfererzes durch Flotation, dann Überführung durch Rösten in Oxid, anschließend Reduktion mit Kohle. Der größte Anteil des produzierten Zinks dient zum Verzinken von Eisenblech für Dachrinnen, Eimer, Drähten und Rohren.
| Dichte / g dm-3: | 7133 | (293 K) |
| 6577 | (m.p.) | |
| Atomvolumen / cm3mol-1: | 9.17 | (293 K) |
| 9.94 | (m.p.) | |
| Elektrische widerstandskraft / µΩcm: | 5.964 | (20 °C) |
| Wärmeleitfähigkeit / W m-1K-1: | 116 |
| Schmelzpunkt / °C: | 419.53 |
| Siedepunkt / °C: | 907 |
| Bildungsenergie / kJ mol-1: | 6.67 |
| Verdampfungsenergie / kJ mol-1: | 114.2 |
| Zerstäubungsenergie / kJ mol-1: | 130.181 |
| Erste ionisierungenergie / kJ mol-1: | 906.41 |
| Zweite ionisierungenergie / kJ mol-1: | 1733.31 |
| Dritte ionisierungenergie / kJ mol-1: | 3832.71 |
| in der Atmosphäre / ppm: | - |
| in der Erdkruste / ppm: | 80 |
| in den Ozeanen / ppm: | 0.01 |
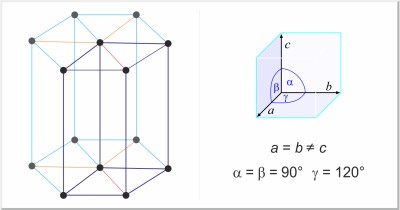
| Kristallstruktur: | hexagonal |
| Gitterparameter der Elementarzelle / pm: | a=266.47, c=494.69 |
| Raumgruppe: | P63/mmc |
| Isotopen | Relative atommasse | Massenanteil (%) |
|---|---|---|
| 64Zn | 63.929147(2) | 48.6(3) |
| 66Zn | 65.926037(2) | 27.9(2) |
| 67Zn | 66.927131(2) | 4.1(1) |
| 68Zn | 67.924848(2) | 18.8(4) |
| 70Zn | 69.925325(4) | 0.6(1) |
| Ausgeglichene halbreaktion | Eo / V | |
|---|---|---|
| Zn2+ + 2e- → Zn(s) | - 0.763 | |
| ZnO22- + 4H+ + 2e- → Zn(s) + 2H2O | +0.441 | |
| HZnO2- + 3H+ + 2e- → Zn(s) + 2H2O | - 0.054 | |
| ZnO22- + 2H2O + 2e- → Zn(s) + 4OH- | - 1.216 | |
| Zn(OH)2(s) + 2e- → Zn(s) + 2OH- | - 1.245 | |
| ZnS(s) + 2e- → Zn(s) + S2- | - 1.40 | |
| Zn(NH3)42+ + 2e- → Zn(s) + 4NH3 | - 1.04 | |
| Zn(CN)42+ + 2e- → Zn(s) + 4CN- | - 1.26 |
| 29 Kupfer | ← | 30 Zink | → | 31 Gallium |
Zitieren dieser Seite:
Generalic, Eni. "Zink." EniG. Periodensystem der Elemente. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/de/zn.html>.
Tabellen und Artikel
- Periodensystem
- Online-Taschenrechner
- Wissenschaftlicher Rechner für Chemiker
- Gasgesetzen Rechner
- Molmassenrechner
- Winkelkonverter
- Römische Zahlen umwandeln
- Numerische Systeme konvertieren
- Herstellung von Lösungen
- Kennzeichnung von Chemikalienbehältern
- Oxidationszahlen Rechner
- ARS methode
- Oxidationszahlmethode
- Ionen-Elektronen-Methode
- Eliminationsmethode von Gauss
- Memory-Spiel
- Paare finden
- Tabellen und Artikel
- Chemie
- Liste mit Akronyme und Abkürzungen
- Kristallsysteme und Bravais-Gitter
- GHS - Gefahrenpiktogramme
- NFPA 704 Gefahrendiamant
- Fundamentale Physikalische Konstanten
- Löslichkeitsprodukt-Konstante
- SI - Internationale Einheitensystem
- Zusammensetzung von Mischungen und Lösungen
- Stöchiometrische Rechnung
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ökologie
- Webdesign
- Chemiewörterbuch (Englisch-Kroatisch)
- Chemie
- Downloads
- ≡ Menü
Copyright © 1998-2025 by Eni Generalic. Alle Rechte vorbehalten. | Bibliographie | Disclaimer
