ANTIMONIO
GRUPO DEL NITRÓGENIO
| Número atómico: | 51 |
| Grupo: | 15 |
| Periodo: | 5 |
| Configuración electrónica: | [Kr] 4d10 5s2 5p3 |
| Estados de oxidación: | -3 +3 +5 |
| Electronegatividad: | 2.05 |
| Radio atómico / pm: | 145 |
| Masa atómica relativa: | 121.760(1) |
El antimonio metálico ya era conocido en la antigüedad por los chinos y babilonios. El origen de la palabra antimonio no está claro: puede proceder p. ej. del griego anti monos (no solo). El símbolo deriva del latín stibium, para nombrar al colorete de antimonio, con el que las mujeres se daban sombra de ojos ya en el antiguo Egipto. Es un semimetal duro y quebradizo, color blanco plateado. Se utiliza en aleaciones con otros metales, para aumentar la dureza y fuerza mecánica de éstos, por ejemplo, el plomo. El antimonio puro se aplica hoy también en la técnica de semiconductores.
| Densidad / g dm-3: | 6691 | (293 K) |
| 6483 | (m.p.) | |
| Volumen molar / cm3mol-1: | 18.20 | (293 K) |
| 18.78 | (m.p.) | |
| Resistencia eléctrica / µΩcm: | 39 | (20 °C) |
| Conductividad térmica / W m-1K-1: | 24.3 |
| Punto de fusión / °C: | 630.63 |
| Punto de ebullición / °C: | 1587 |
| Calor de fusión / kJ mol-1: | 20.9 |
| Calor de vaporización / kJ mol-1: | 165.8 |
| Calor de atomización / kJ mol-1: | 262.04 |
| Primera energía de ionización / kJ mol-1: | 830.59 |
| Segunda energía de ionización / kJ mol-1: | 1594.96 |
| Tercera energía de ionización / kJ mol-1: | 2441.10 |
| en la atmósfera / ppm: | - |
| en la corteza terrestre / ppm: | 0.2 |
| en los océanos / ppm: | 0.0005 |
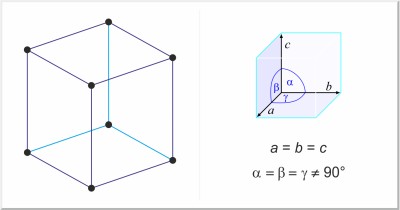
| Estructura cristalina: | romboédrica |
| Dimensiones de la celda unidad / pm: | a=430.84, c=1124.7 |
| Grupo espacial: | R3m |
| Isótopo | Masa atómica relativa | Porcentaje por masa (%) |
|---|---|---|
| 121Sb | 120.903818(2) | 57.36(8) |
| 123Sb | 122.904216(2) | 42.64(8) |
| Semirreacción | Eo / V | |
|---|---|---|
| SbV + 2e- → SbIII | +0.818 | (6 mol dm-3 HCl) |
| SbV + 2e- → SbIII | +0.746 | (3.5 mol dm-3 HCl) |
| SbO+ + 2H+ + 3e- → Sb(s) + H2O | +0.212 | |
| SbO3- + 2H+ + 2e- → SbO2- + H2O | +0.353 | |
| SbO3- + 3H+ + 2e- → HSbO2 + H2O | +0.678 | |
| SbO3- + 4H+ + 2e- → SbO+ + 2H2O | +0.704 | |
| SbO2- + 2H+ + 2e- → SbO- + H2O | +0.720 | |
| 2SbO3- + 6H+ + 4e- → Sb2O3(s) + 3H2O | +0.772 | |
| SbO2- + 4H+ + 3e- → Sb(s) + 2H2O | +0.446 | |
| HSbO2 + 3H+ + 3e- → Sb(s) + 2H2O | +0.230 | |
| Sb2O3(s) + 6H+ + 6e- → 2Sb(s) + 3H2O | +0.152 | |
| Sb2O5(s) + 6H+ + 4e- → 2SbO+ + 3 H2O | +0.581 | |
| Sb2O5(s) + 4H+ + 4e- → Sb2O3(s) + 2H2O | +0.692 | |
| Sb(s) + 3H+ + 3e- → SbH3(g) | - 0.510 |
| 50 Estaño | ← | 51 Antimonio | → | 52 telurio |
Citación de esta página:
Generalic, Eni. "Antimonio." EniG. Tabla periódica de los elementos. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/es/sb.html>.
Tablas y artículos
- Tabla periódica
- Calculadoras online
- Calculadora científica para química
- Calculadora con leyes de los gases
- Calculadora de masa molar
- Convertir ángulo
- Convertidor números romanos
- Sistema de numeración convertidor
- Preparación de las soluciones
- Etiquetado de envases químicos
- Calculadora de números de oxidacion
- ARS metodo
- Método del número de oxidación
- Método del ion-electrón
- Método de eliminación de Gauss
- Juego de memoria
- Encuentre los pares
- Tablas y artículos
- Química
- Lista de acrónimos y abreviaturas
- Sistemas cristalinos y redes de Bravais
- SGA - Pictogramas de peligro
- Diamante de peligro de NFPA 704
- Constantes físicas fundamentales
- Constantes del producto de solubilidad
- SI - Sistema Internacional de Unidades
- Composición de mezclas y soluciones
- Cálculo estequiométrico
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ecología
- Diseño web
- Diccionario de química (inglés-croata)
- Química
- Descargas
- ≡ Menú
