ARGENT
ÉLÉMENT de TRANSITION: GROUPE du CUIVRE
| Nombre atomique: | 47 |
| Groupe: | 11 |
| Période: | 5 |
| Configuration électronique: | [Kr] 4d10 5s1 |
| Nombre d'oxydation: | +1 |
| Électronégativité: | 1.93 |
| Rayon atomique / pm: | 144.5 |
| Masse atomique relatives: | 107.8682(2) |
L'argent est connu depuis la haute antiquité. Étymologie du nom: vient du latin argentum signifiant argent. L'argent est un métal argenté, malléable et ductile. Il ne réagit ni avec l'eau, ni avec l'oxygène. Il réagit avec les composés soufrés pour former des sulfates. On trouve l'argent dans des minerais appelés argentite (AgS), proustite (Ag3AsS3), pyrargyrite (Ag3SbS3). Les alliages d'argent sont utilisés en joaillerie. Dans d'autres composés, il est utilisé en photographie. C'est un bon conducteur. Il est assez cher.
| Densité / g dm-3: | 10500 | (293 K) |
| 9345 | (m.p.) | |
| Volume molaire / cm3mol-1: | 10.27 | (293 K) |
| 11.54 | (m.p.) | |
| Résistivité électrique / µΩcm: | 1.59 | (20 °C) |
| Conductibilité thermique / W m-1K-1: | 429 |
| Point de fusion / °C: | 961.78 |
| Point d'ébullition / °C: | 2162 |
| Enthalpie de fusion / kJ mol-1: | 11.3 |
| Enthalpie d'évaporation / kJ mol-1: | 257.7 |
| Chaleur d'atomisation / kJ mol-1: | 284.09 |
| Energie de première ionisation / kJ mol-1: | 731.01 |
| Energie de deuxième ionisation / kJ mol-1: | 2073.48 |
| Energie de troisième ionisation / kJ mol-1: | 3360.61 |
| dans l'atmosphère / ppm: | - |
| dans la croute terrestre / ppm: | 0.08 |
| dans les océans / ppm: | 0.0003 |
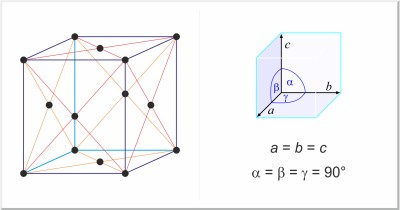
| Structure cristalline: | cubique à faces centrées |
| Dimension de la cellule unitaire / pm: | a=408.626 |
| Groupe d'espace: | Fm3m |
| Isotope | Masse atomique relatives | Pourcentage massique (%) |
|---|---|---|
| 107Ag | 106.905093(6) | 51.839(7) |
| 109Ag | 108.904756(3) | 48.161(7) |
| Demi-réaction | Eo / V | |
|---|---|---|
| Ag+ + e- → Ag(s) | +0.799 | |
| Ag+ + e- → Ag(s) | +0.228 | (1 mol dm-3 HCl) |
| Ag+ + e- → Ag(s) | +0.792 | (1 mol dm-3 HClO4) |
| Ag+ + e- → Ag(s) | +0.77 | (1 mol dm-3 H2SO4) |
| Ag2+ + e- → Ag+ | +1.998 | |
| AgO+ + 2H+ + e- → Ag2+ + H2O | +2.016 | |
| 2AgO(s) + 2H+ + 2e- → Ag2O + H2O | +1.41 | |
| 2AgO(s) + H2O + 2e- → Ag2O + OH- | +0.599 | |
| Ag2O(s) + 2H+ + 2e- → 2Ag(s) + H2O | +1.173 | |
| Ag2O(s) + H2O + 2e- → 2Ag(s) + 2OH- | +0.342 | |
| Ag2CrO4(s) + 2e- → 2Ag(s) + CrO42- | +0.446 | |
| Ag2S(s) + 2H+ + 2e- → 2Ag(s) + H2S(g) | - 0.036 | |
| Ag2S(s) + 2e- → 2Ag(s) + S2- | - 0.712 | |
| AgCl(s) + e- → Ag(s) + Cl- | +0.222 | |
| AgCl(s) + e- → Ag(s) + Cl- | +0.228 | (1 mol dm-3 KCl) |
| AgBr(s) + e- → Ag(s) + Br- | +0.073 | |
| AgI(s) + e- → Ag(s) + I- | - 0.151 | |
| Ag(CN)2- + e- → Ag(s) + 2CN- | - 0.31 | |
| Ag(S2O3)23- + e- → Ag(s) + 2S2O32- | +0.017 |
| 46 Palladium | ← | 47 Argent | → | 48 Cadmium |
Citation de cette page:
Generalic, Eni. "Argent." EniG. Tableau périodique des éléments. KTF-Split, 13 Feb. 2025. Web. 31 Mar. 2025. <https://www.periodni.com/fr/ag.html>.
Tableaux et articles
- Tableau périodique
- Home
- Forme courte du tableau périodique
- Forme longue du tableau périodique
- History of the Periodic table of elements
- Impression du tableau périodique
- Configuration électronique des éléments
- Liste alphabétique des éléments chimiques
- Naming of elements of atomic numbers greater than 100
- ASCII Tableau périodique
- Calculatrices online
- Calculatrice scientifique pour chimiste
- Calculatrice lois de gaz
- Calculateur de masse molaire
- Convertir angle
- Convertisseur chiffres romains
- Convertisseur systèmes numériques
- Préparation des solutions
- Étiquetage des conteneurs chimiques
- Calculateur de nombres d'oxydation
- ARS methode
- Méthode du changement des nombres d'oxydation
- Méthode ions-électrons
- Méthode d'élimination de Gauss
- Jeu de mémoire
- Trouvez les paires
- Tableaux et articles
- Chimie
- Liste des abréviations et acronymes
- Systèmes cristallins et réseaux de Bravais
- SGH - Pictogrammes de danger
- NFPA 704 feu diamant
- Constantes physiques fondamentales
- Constantes du produit de solubilité
- SI - Système international d'unités
- Composition des melanges et des solutions
- Calcul stœchiométrique
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Écologie
- Web design
- Dictionnaire de chimie (anglais-croate)
- Chimie
- Télécharger
- ≡ Menu
