KISIK
HALKOGENI ELEMENT
| Atomski broj: | 8 |
| Skupina: | 16 |
| Perioda: | 2 |
| Elektronska konfiguracija: | [He] 2s2 2p4 |
| Oksidacijski broj: | -2 |
| Elektronegativnost: | 3.44 |
| Atomski radijus / pm: | 60.4 |
| Relativna atomska masa: | [15.999 03, 15.999 77] |
Kisik je 1772. godine otkrio Carl William Scheele (SE). Ime je dobio od Lavoisiera koji mu je dao ime oxygene od grčke riječi oxys što znači oštar ili kiseo i riječi genes što znači tvoriti. To je plin bez boje i mirisa i ekstremno je reaktivan. Stvara okside sa svim ostalim elementima izuzev plemenitih plinova. Kisik je nezapaljivi plin ali podržava gorenje. Nešto je teži od zraka i dobro se otapa u vodi, topljivost mu je oko 3 % (volumna). Javlja se u dvije alotropske modifikacije, kao dvoatomne i kao troatomne molekule (ozon). I jedna i druga su jaka oksidacijska sredstva. Topljivost ozona u vodi je gotovo 50 puta veća nego topljivost dvoatomnog kisika. Kisik je najrasprostranjeniji element Zemljine kore. Skoro polovica mase je kisik, a po broju atoma je brojniji nego svi ostali elementi zajedno. Kisik se industrijski dobiva ili frakcijskom destilacijom ukapljenog zraka ili elektrolizom vode. Najčešće se upotrebljava kao oksidacijsko sredstvo. Cijena plinovitog kisika čistoće 99.99% iznosi 188.90 €/dm3 u malim pakovanjima (1 dm3) i oko 1.46 €/dm3 u velikom pakovanju (300 dm3).
| Gustoća / g dm-3: | 2000 | (čvrsto stanje, t.t.) |
| 1140 | (t.v.) | |
| 1.429 | (plinovito stanje, 273 K) | |
| Molarni volumen / cm3mol-1: | 8.00 | (čvrsto stanje, t.t.) |
| 14.03 | (t.v.) | |
| 22392.44 | (plinovito stanje, 273 K) | |
| Električna otpornost / µΩcm: | - | (20 °C) |
| Toplinska vodljivost / W m-1K-1: | 0.0263 |
| Temperatura taljenja / °C: | -218.7916 |
| Temperatura vrenja / °C: | -182.95 |
| Toplina taljenja / kJ mol-1: | 0.444 |
| Toplina isparavanja / kJ mol-1: | 6.82 |
| Toplina atomiziranja / kJ mol-1: | 246.785 |
| Prva energija ionizacije / kJ mol-1: | 1313.95 |
| Druga energija ionizacije / kJ mol-1: | 3388.33 |
| Treća energija ionizacije / kJ mol-1: | 5300.51 |
| u atmosferi / ppm: | 209500 |
| u Zemljinoj kori / ppm: | 466000 |
| u oceanima / ppm: | (H2O) |
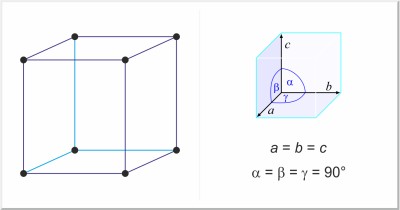
| Kristalna struktura: | jednostavna kubična |
| Dimenzije jedinične ćelije / pm: | a=683 |
| Prostorna grupa: | Pm3n |
| Izotop | Relativna atomska masa | Maseni udio (%) |
|---|---|---|
| 16O | 15.994914622(2) | 99.762(15) |
| 17O | 16.9991315(2) | 0.038(3) |
| 18O | 17.9991604(9) | 0.200(12) |
| Uravnotežena polureakcija | Eo / V | |
|---|---|---|
| O2(g) + 4H+ + 4e- → 2H2O | +1.229 | |
| O2(g) + 4H+ + 4e- → 2H2O | +0.815 | ([H+] = 10-7 mol dm-3) |
| O2(g) + 2H2O + 4e- → 4OH- | +0.401 | |
| O2(g) + H2O + 2e- → HO2- + OH- | +0.076 | |
| O2(g) + 2H+ + 2e- → H2O2 | +0.682 | |
| O3(g) + 2H+ + 2e- → O2(g) + H2O | +2.07 | |
| O3(g) + 6H+ + 6e- → 3H2O | +1.501 | |
| O3(g) + H2O + 2e- → O2(g) + 2OH- | +1.24 | |
| HO2- + H2O + 2e- → 3OH- | +0.88 | |
| H2O2 + 2H+ + 2e- → 2H2O | +1.776 |
Citiranje ove stranice:
Generalić, Eni. "Kisik." EniG. Periodni sustav elemenata. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/hr/o.html>.
Članci i tablice
- Periodni sustav
- Home
- Kratki oblik tablice periodnog sustava
- Dugi oblik tablice periodnog sustava
- Povijest periodnog sustava kemijskih elemenata
- Printabilni periodni sustav
- Elektronske konfiguracije elemenata
- Abecedni popis kemijskih elemenata
- Imenovanje elemenata s atomskim brojem većim od 100
- ASCII Periodni sustav
- Online kalkulatori
- Znanstveno računalo (kalkulator) za kemičare
- Kalkulator plinskih zakona
- Kalkulator molarne mase
- Pretvaranje kutova
- Pretvaranje rimskih brojeva u arapske
- Pretvaranje brojevnih sustava
- Priprema otopina
- Označavanje kemijskih posuda
- Kalkulator oksidacijskih brojeva
- ARS metoda
- Metoda promjene oksidacijskih brojeva
- Ion-elektron metoda
- Gaussova metoda eliminacije
- Igra memorije
- Pronađi parove
- Članci i tablice
- Kemija
- Lista kratica i akronima
- Kristalni sustavi i Bravaisove rešetke
- GHS - Piktogrami opasnosti
- NFPA 704 dijamant opasnosti
- Temeljne fizikalne konstante
- Konstante produkta topljivosti
- SI - Međunarodni sustav mjernih jedinica
- Sastav smjesa i otopina
- Stehiometrijski račun
- Klorinitet i slanost mora
- Elementi rijetkih zemalja (REE)
- Izjednačavanje kemijskih jednadžbi
- Teorija valentne veze
- Ekologija
- Web dizajn
- Kemijski rječnik
- Kemija
- Download
- ≡ Meni
