Cl
Chlorum
CLORO
ALOGENI ELEMENTI
| Numero atomico: | 17 |
| Gruppo: | 17 |
| Periodo: | 3 |
| Configurazione elettronica: | [Ne] 3s2 3p5 |
| Numeri di ossidazione: | -1 +1 +5 +7 |
| Elettronegatività: | 3.16 |
| Raggio atomico / pm: | 99.4 |
| Massa atomica relativa: | [35.446, 35.457] |
Scopritore:1774 Carl William Scheele (SE)
Il cloro deriva dal Greco chloros (giallo-verdastro). Il nome richiama la caratterisitca cromatica a temperatura e pressione ambiente di questo gas, tossico e irritante, che si presenta appunto con una colorazione giallo-verde. È il non si trova libero in natura; si trova in molti minerali. Industrialmente si prepara per elettrolisi di una soluzione acquosa di NaCl. Usato come disinfettante nel trattamento delle acque, come sbiancante. Entra nella composizione di materiali plastici (es. PVC).
| Densità / g dm-3: | 2030 | (113 K) |
| 1507 | (239 K) | |
| 3.214 | (273 K) | |
| Volume atomico / cm3mol-1: | 17.46 | (113 K) |
| 23.53 | (239 K) | |
| 22061.61 | (273 K) | |
| Resistività Elettrica / µΩcm: | - | (20 °C) |
| Conducibilità termica / W m-1K-1: | 0.0089 |
| Temperatura di fusione / °C: | -101.5 |
| Temperatura di ebollizione / °C: | -34.04 |
| Calore di fusione / kJ mol-1: | 6.41 |
| Calore di vaporizzazione / kJ mol-1: | 20.4033 |
| Calore di atomizzazione / kJ mol-1: | 120 |
| Energia di prima ionizzazione / kJ mol-1: | 1251.20 |
| Energia di seconda ionizzazione / kJ mol-1: | 2297.72 |
| Energia di terza ionizzazione / kJ mol-1: | 3821.81 |
| nell'atmosfera / ppm: | - |
| nella crosta terrestre / ppm: | 130 |
| negli oceani / ppm: | 19000 |
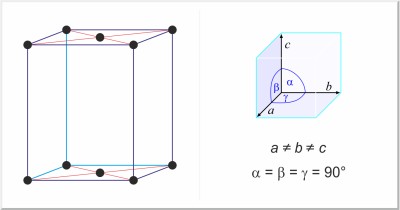
| Struttura cristallina: | ortorombico a base centrata |
| Dimensioni della cella unitaria / pm: | a=624, b=448, c=826 |
| Gruppo spaziale: | Cmca |
| Isotopo | Massa atomica relativa | Percentuale in peso (%) |
|---|---|---|
| 35Cl | 34.96885271(4) | 75.77(7) |
| 37Cl | 36.96590260(5) | 24.23(7) |
| Bilanciamento della semireazione | Eo / V | |
|---|---|---|
| Cl2(g) + 2e- → 2Cl- | +1.359 | |
| Cl2(aq) + 2e- → 2Cl- | +1.39 | |
| ClO4- + 2H+ + 2e- → ClO3- + H2O | +1.19 | |
| ClO4- + H2O + 2e- → ClO3- + 2OH- | +0.36 | |
| 2ClO4- + 16H+ + 14e- → Cl2(g) + 8H2O | +1.39 | |
| ClO3- + 3H+ + 2e- → HClO2 + H2O | +1.21 | |
| ClO3- + H2O + 2e- → ClO2- + 2OH- | +0.33 | |
| 2ClO3- + 12H+ + 10e- → Cl2(g) + 3H2O | +1.47 | |
| HClO2 + 2H+ + 2e- → HClO + H2O | +1.64 | |
| ClO2- + H2O + 2e- → ClO- + 2OH- | +0.66 | |
| 2HClO + 2H+ + 2e- → Cl2(g) + H2O | +1.63 | |
| 2ClO- + 2H2O + 2e- → Cl2(g) + 4OH- | +0.40 |
Citazione della questa pagina:
Generalic, Eni. "Cloro." EniG. Tavola periodica degli elementi. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/it/cl.html>.
Tavoli e articoli
- Tavola periodica
- Home
- Forma breve della tavola periodica
- Forma lunga della tavola periodica
- History of the Periodic table of elements
- Tavola periodica stampabile
- Configurazione elettronica degli elementi
- Elenco alfabetico degli elementi chimici
- Naming of elements of atomic numbers greater than 100
- ASCII Tavola periodica
- Calcolatrici online
- Calcolatrice scientifica per i chimici
- Calcolatrice di leggi dei gas
- Calcolatore della massa molare
- Convertitore angolo
- Convertitore di numeri romani
- Convertitore sistemi numerazione
- Preparazione delle soluzioni
- Etichettatura dei contenitori chimici
- Calcolatrice numeri di ossidazione
- ARS metodo
- Metodo della variazione del numero di ossidazione
- Metodo ione-elettrone
- Metodo di eliminazione di Gauss
- Gioco di memoria
- Trova le coppie
- Tabelle e articoli
- Chimica
- Lista di abbreviazioni e acronimi
- Sistemi cristallini e reticoli di Bravais
- GHS - Pittogrammi di pericolo
- Diamante di fuoco di NFPA 704
- Costanti fisiche fondamentali
- Costanti del prodotto di solubilità
- SI - Unità del Sistema Internazionale
- Composizione delle miscele e soluzioni
- Calcolo stechiometrico
- Chlorinity and salinity of seawater
- Elementi di terre rare (REE)
- Ecologia
- Web design
- Dizionario di chimica (inglese-croato)
- Chimica
- Scaricare
- ≡ Menu
Copyright © 1998-2025 by Eni Generalic. Tutti i diritti sono riservati. | Bibliografia | Disclaimer
