MANGAN
UEBERGANGSELEMENTE: MANGANGRUPPE
| Ordnungszahl: | 25 |
| Elementgruppen: | 7 |
| Perioden: | 4 |
| Elektronenkonfiguration: | [Ar] 3d5 4s2 |
| Oxidationszustände: | +2 +3 +4 +7 |
| Elekronegativität: | 1.55 |
| Atomradius / pm: | 136.7 |
| Relative atommasse: | 54.938 044(3) |
Endeckung:1774 Johan Gottlieb Gahn (SE)
Der Name Mangan kommt vom von französischen Wort manganèse (schwarze Magnesia). Es ist ein stahlgraues, sehr hartes und sprödes Schwermetall. Es tritt in der Natur nicht elementar auf, kommt aber in zahlreichen Erzen in chemisch gebunder Form vor. Die Herstellung erfolgt in der Technik durch die Reduktion von Pyrolusit mit Silicium. Manganstähle mit hohem Mangangehalt sind enorm zäh, schmiedbar, härtbar und wärmebeständig. Sie kommen in Baggerzähnen, Schienen, Weichen, Gewindebohrern und Schneidewerkzeugen zum Einsatz.
| Dichte / g dm-3: | 7440 | (alpha, 293 K) |
| 6430 | (m.p.) | |
| Atomvolumen / cm3mol-1: | 7.38 | (alpha, 293 K) |
| 8.54 | (m.p.) | |
| Elektrische widerstandskraft / µΩcm: | 144 | (20 °C) |
| Wärmeleitfähigkeit / W m-1K-1: | 7.82 |
| Schmelzpunkt / °C: | 1246 |
| Siedepunkt / °C: | 2061 |
| Bildungsenergie / kJ mol-1: | 14.4 |
| Verdampfungsenergie / kJ mol-1: | 220.5 |
| Zerstäubungsenergie / kJ mol-1: | 279.37 |
| Erste ionisierungenergie / kJ mol-1: | 717.28 |
| Zweite ionisierungenergie / kJ mol-1: | 1509.04 |
| Dritte ionisierungenergie / kJ mol-1: | 3248.49 |
| in der Atmosphäre / ppm: | - |
| in der Erdkruste / ppm: | 1400 |
| in den Ozeanen / ppm: | 0.002 |
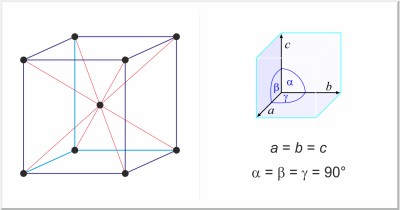
| Kristallstruktur: | kubisch-raumzentriert |
| Gitterparameter der Elementarzelle / pm: | a=891.39 |
| Raumgruppe: | I43m |
| Isotopen | Relative atommasse | Massenanteil (%) |
|---|---|---|
| 55Mn | 54.938050(1) | 100 |
| Ausgeglichene halbreaktion | Eo / V | |
|---|---|---|
| MnIV + e- → MnIII | +1.65 | (14 mol dm-3 H2SO4) |
| MnIII + e- → MnII | +1.59 | (14 mol dm-3 H2SO4) |
| Mn3+ + e- → Mn2+ | +1.51 | (7.5 mol dm-3 H2SO4) |
| Mn2+ + 2e- → Mn(s) | - 1.180 | |
| MnO4- + e- → MnO42- | +0.564 | |
| MnO4- + 2H2O + 3e- → MnO2(s) + 4OH- | +0.588 | |
| MnO4- + 4H+ + 3e- → MnO2(s) (alpha) + 2H2O | +1.695 | |
| MnO4- + 4H+ + 3e- → MnO2(s) (beta) + 2H2O | +1.679 | |
| MnO4- + 8H+ + 4e- → Mn3+ + 4H2O | +1.506 | |
| MnO4- + 8H+ + 5e- → Mn2+ + 4H2O | +1.51 | |
| MnO42- + 4H+ + 2e- → MnO2(s) + 2H2O | +2.257 | |
| MnO42- + 5H+ + 2e- → HMnO2- + 2H2O | +1.234 | |
| MnO42- + 2H2O + 2e- → MnO2(s) + 4OH- | +0.51 | (18 °C) |
| MnO2(s) + 4H+ + e- → Mn3+ + 2H2O | +0.948 | |
| MnO2(s) (alpha) + 4H+ + 2e- → Mn2+ + 2H2O | +1.23 | |
| MnO2(s) (beta) + 4H+ + 2e- → Mn2+ + 2H2O | +1.22 | |
| MnO2(s) (gamma) + 4H+ + 2e- → Mn2+ + 2H2O | +0.21 | |
| Mn(OH)3(s) + e- → Mn(OH)2(s) + 2OH- | +0.1 | |
| Mn(CN)63- + e- → Mn(CN)64- | - 0.244 | |
| Mn(OH)2(s) + 2e- → Mn(s) + 2OH- | - 1.55 | |
| HMnO2- + 3H+ + 2e- → Mn(s) + 2H2O | - 0.163 |
Zitieren dieser Seite:
Generalic, Eni. "Mangan." EniG. Periodensystem der Elemente. KTF-Split, 13 Feb. 2025. Web. 30 Mar. 2025. <https://www.periodni.com/de/mn.html>.
Tabellen und Artikel
- Periodensystem
- Online-Taschenrechner
- Wissenschaftlicher Rechner für Chemiker
- Gasgesetzen Rechner
- Molmassenrechner
- Winkelkonverter
- Römische Zahlen umwandeln
- Numerische Systeme konvertieren
- Herstellung von Lösungen
- Kennzeichnung von Chemikalienbehältern
- Oxidationszahlen Rechner
- ARS methode
- Oxidationszahlmethode
- Ionen-Elektronen-Methode
- Eliminationsmethode von Gauss
- Memory-Spiel
- Paare finden
- Tabellen und Artikel
- Chemie
- Liste mit Akronyme und Abkürzungen
- Kristallsysteme und Bravais-Gitter
- GHS - Gefahrenpiktogramme
- NFPA 704 Gefahrendiamant
- Fundamentale Physikalische Konstanten
- Löslichkeitsprodukt-Konstante
- SI - Internationale Einheitensystem
- Zusammensetzung von Mischungen und Lösungen
- Stöchiometrische Rechnung
- Chlorinity and salinity of seawater
- Rare earth elements (REE)
- Ökologie
- Webdesign
- Chemiewörterbuch (Englisch-Kroatisch)
- Chemie
- Downloads
- ≡ Menü
